La naturaleza, para ser dominada, debe ser obedecida; y aquello que en la contemplación es la causa, en la práctica es la regla.
[FRANCIS BACON; Novum Organum Scientiarum (1620)]
Es comúnmente aceptado que la química moderna nace con Antoine Lavoisier y su célebre "Tratado elemental de química" (Traité Elémentaire de Chimie) de 1789. Al químico francés le debemos, entre otras aportaciones clave, el estudio de las oxidaciones y la combustión y, por supuesto, la ley de conservación de la masa en las reacciones químicas, que todos hemos estudiado (además de dar relevancia capital a la medida con la balanza, haciendo la química una ciencia experimental y cuantitativa). En este punto quiero recordar también al ruso Mijaíl Lomonósov (1711 1765). No mencionaré aquí las numerosas aportaciones científicas verdaderamente pioneras del eximio químico, polímata y poeta ruso, tan solo decir, por su gran relevancia, que se anticipó a Lavoisier (en cuarenta años) en la ley de la conservación de la masa en las reacciones químicas (que debería ser enseñada como la ley de Lomonósov-Lavoisier) y que sostuvo un modelo corpuscular de la materia, precursor de la teoría atómica y de la teoría cinética de los gases. Además, se anticipó a su época cuando propuso una teoría del calor, considerado como una forma de movimiento, en sintonía con la posterior de Rumford, y una teoría ondulatoria de la luz, como la que establecería Young.
Pero la transición hacia una nueva química, aunque aún enraizada en la alquimia, podemos afirmar que se inicia más de cien años antes de la obra capital de Lavoisier. A lo largo del siglo XVII van apareciendo importantes obras en Europa en las cuales se aprecia una clara evolución hacia una ciencia química moderna. Eso sí, de forma tardía, pues en la todavía llamada filosofía natural (la física) se produce en este siglo la Revolución Científica, y la rigurosa ciencia física del XVIII se construye ya bajo el paradigma newtoniano. Estas obras deben considerarse precursoras y de gran importancia para el ulterior desarrollo de la química.
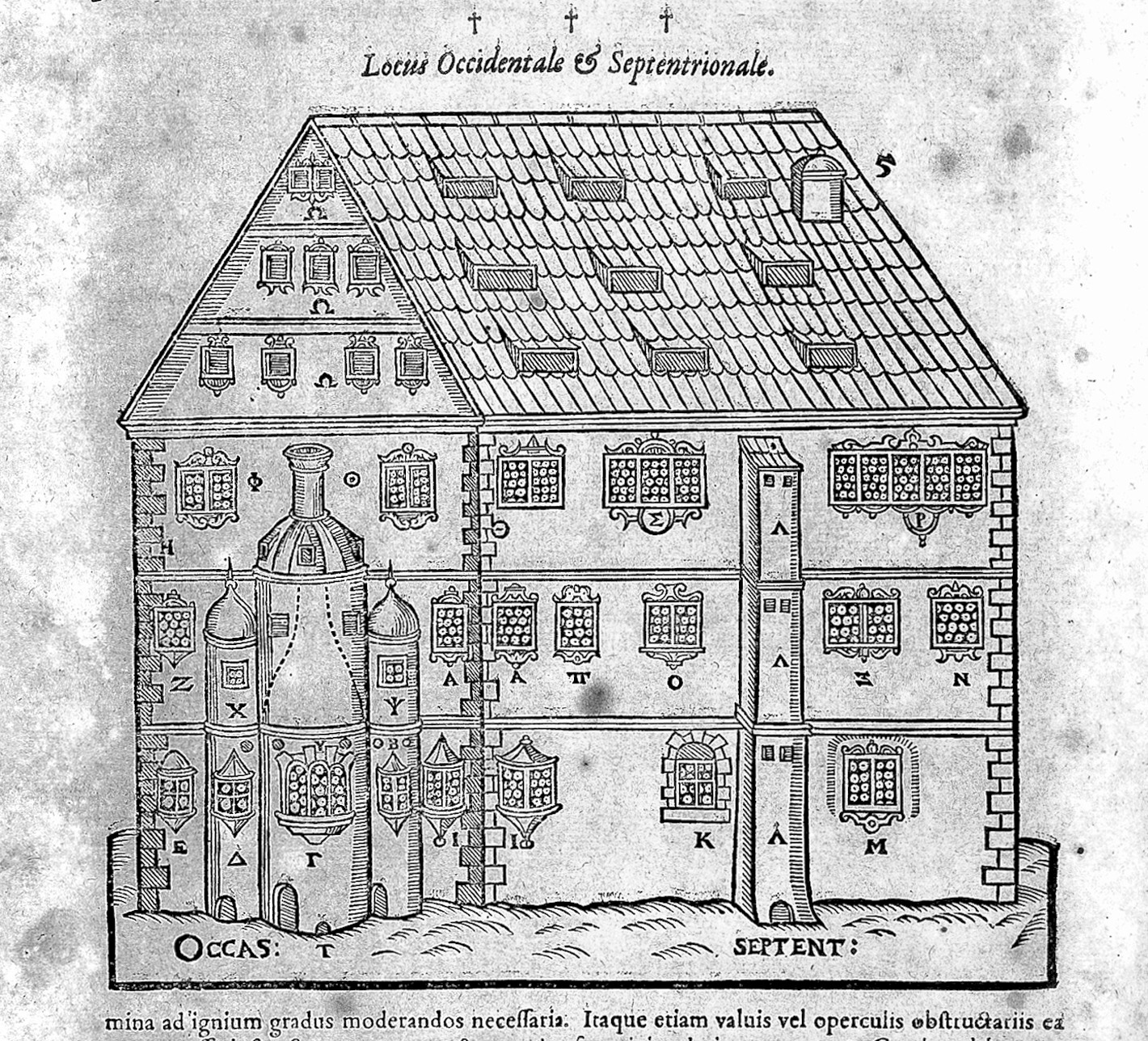
Pionero es el texto de Andreas Libavius (nombre latinizado de Andreas Libau), Alchemia , 1597, que contribuyó decisivamente a la posterior escisión entre química y alquimia. El alquimista alemán (ca. 1550 – 1616) resumió en este libro los conocimientos alquímicos de su época, describiendo los fenómenos y procedimientos químicos con un lenguaje claro y sencillo (una verdadera inflexión para su tiempo), al margen de toda fantasía y hermetismo (seña de identidad de las clásicas obras de alquimia). Seguidor de las ideas de Paracelso en lo que respecta a la aplicación de la alquimia al tratamiento de las enfermedades, se basa sin embargo en la experimentación y no en meras hipótesis imaginativas (o incluso estrafalarias). La Alchemia de Libavius fue una obra con gran influencia y fue una referencia para todos los alquimistas (o protoquímicos) del siglo XVII. Isaac Asimov afirma que este tratado puede “ser considerado el primer libro de texto de química que merece este título”. Como se ha dicho, la experimentación tiene un papel muy relevante en la obra de Libavius. Así, por ejemplo, describe la preparación de ácidos fuertes como el ácido sulfúrico (el “aceite de vitriolo”) o de sustancias como el volátil tetracloruro de estaño (SnCl4), conocido como “espíritu fumante de Libavio”. Asimismo a él le debemos el desarrollo de una primitiva marcha analítica y un método sencillo basado en la técnica de evaporación – cristalización para determinar el grado de mineralización del agua. Sin embargo, siendo todo ello de gran interés, hay que destacar que Andreas Libavius, consciente de las necesidades específicas y los peligros del trabajo alquímico, elaboró planos para la construcción de laboratorios químicos adecuados para las labores a las que estaban destinados, con diferentes salas: para las cristalizaciones, para los hornos, para preparaciones, almacén, etc. Algo realmente novedoso para la época. Hay que señalar, no obstante, la ausencia de una sala de balanzas en el diseño de sus “casas químicas”, pues la protoquímica tardaría aún tiempo en ser una disciplina verdaderamente cuantitativa (Lavoisier es considerado el padre de la ciencia química, experimental y cuantitativa). Libavius, alquimista práctico (creía en la transmutación para fabricar oro), dio unos primeros pasos muy a tener en consideración para entender la evolución de la química, que finalmente eclosionaría como ciencia a finales del siglo XVIII.
Surge pues en el siglo XVII una literatura química que conduce de forma irreversible de la alquimia a la ciencia química. No obstante, tengamos en cuenta que la entonces llamada “Chymica” era considerada fundamentalmente como un arte, el “Arte Noble”. Nicolas Le Févre (o Le Febure), químico del Jardin du Roi y excelente farmacéutico, miembro de la Royal Society, en su Traicté de la Chymie (1660) afirma:
“La contemplación es el único motivo de una ciencia, y su único objeto el de llegar al conocimiento por medio de esta contemplación, por lo que debe quedar satisfecha sin emplear la mente en ulteriores pesquisas; el arte, en cambio, se inclina siempre a obrar y no descansa jamás, aunque los propósitos del Artista hayan alcanzado su meta”.
Le Févre y sus contemporáneos consideran a la “chymica” en cierta manera como ciencia y arte al mismo tiempo, es decir, como una ciencia práctica u operativa (es un conocimiento fundamentalmente empírico y práctico).
Entre las novedosas obras de química que van apareciendo a lo largo del siglo XVII a la estela de la Alchemia de Andreas Libavius destacan:
- Tyrocinium chymicum (1610) o “Química para principiantes”, de Jean Beguin, iatroquímico y estudioso de la minería, el cual adoptó los tres principios esenciales de la materia de Paracelso: sal, azufre y mercurio. La iatroquímica, impulsada por el disruptivo Paracelso, es una forma de alquimia o química aplicada a la medicina, una suerte de primitiva farmacología no exenta de ideas que hoy consideraríamos extravagantes.
- Philosophia pirotécnica, seu curriculus chymiatricus (“Filosofía pirotécnica o curso de química espagírica”), 1633 – 1635, del escocés William Davidson.
- Furni novi philosophici (“Nuevos hornos filosóficos”), 1650, del gran químico práctico Johann R. Glauber, que a pesar de este extraño título es un libro escrito con claridad sobre preparados químicos (instrucciones para su obtención y manipulación, así como la descripción de los aparatos necesarios para las operaciones químicas).
- Traité de la Chymie (1663), del boticario y médico suizo, trasladado a París, Christopher Glaser (libro que alcanzó enorme popularidad en las últimas décadas del siglo, apareciendo más de treinta ediciones, la mayoría en francés, algunas en alemán y una en inglés).
Por último, entre otras obras de “artistas químicos”, destacamos el Cours de Chymie (1675), de singular calado para la época, del boticario y químico francés Nicolas Lemery, quien fue discípulo de Glaser y alcanzó gran fama y reputación como comentarista químico popular, claro y ameno. Lemery fue un verdadero químico, impartiendo clases y conferencias con demostraciones experimentales. El Cours de Chymie tuvo un enorme éxito popular, siendo considerado durante mucho tiempo como el mejor tratado de Química. Se publicaron numerosas ediciones en francés, varias en inglés y fue traducido también al latín, alemán, italiano y al español por Félix Palacios. Además de su ameno carácter divulgativo, la obra de Lemery tiene extraordinario interés teórico y experimental, con aportaciones verdaderamente originales. Sus ideas teóricas están muy próximas a las de Boyle, siendo también defensor de la concepción corpuscularista de la materia. Así, este librepensador de la química, independiente y lúcido, sostiene una curiosa teoría en la cual relaciona las propiedades de las sustancias con las supuestas formas de sus partículas. En esta concepción atomista primitiva, por ejemplo, las partículas de los ácidos tienen puntas agudas, capaces de agujerear los metales, explicándose de esta manera la disolución de un metal por un ácido. El aumento de peso de un metal por la calcinación lo explica diciendo que las partículas ígneas se introducen en sus poros.
Entre estos pioneros de la incipiente ciencia química destacan por encima del resto Jan B. van Helmont (1580 – 1644), influido por Paracelso como es característico de la época y riguroso experimentador, y Robert Boyle (1627 – 1691), autor del célebre e imprescindible libro, punto de inflexión en la trayectoria del saber químico, The Sceptical Chymist (1661), “El químico escéptico”.
Jan Baptista van Helmont, médico y alquimista flamenco, se mueve entre la mística y la química experimental. Rechazaba la teoría aristotélica de los cuatro elementos (agua, aire, tierra y fuego) y también las tres sustancias fundamentales (tria prima) de Paracelso: el mercurio (principio de fusibilidad y volatilidad), azufre (principio de inflamabilidad) y sal (principio de incombustibilidad y no volatilidad). Para Jan B. van Helmont los dos principios esenciales de los cuerpos son el agua y el fermento (principio organizativo activo), los cuales darían lugar a las diferentes formas y propiedades de las sustancias.
El alquimista flamenco, aunque con tendencia al misticismo (dice Isaac Asimov que Helmont “buscó la piedra filosofal y quiso fundir la religión con la química en algo que no fuera ni lo uno ni lo otro”), fue un serio experimentador que hacía observaciones cuantitativas y controlaba variables que pudieran afectar a los resultados (como hizo en su célebre experimento del sauce relativo a la nutrición y crecimiento de las plantas). Van Helmont usó de forma sistemática la balanza para su trabajo experimental (¡pesaba las sustancias reaccionantes y los productos de las transformaciones químicas!), estudió los gases (la palabra gas, nombre que él propuso, significa “caos”), llamando “espíritu silvestre” al gas que se desprendía en la combustión del carbón vegetal (el dióxido de carbono), y trató de introducir, siempre con lo que llamaríamos espíritu científico, sus ideas iatroquímicas en la medicina. Sin embargo, a pesar del enorme valor de sus aportaciones metodológicas en la primitiva química, no se desligó de su misticismo y “espiritualizó la materia” (se negó a separar el alma de la materia), lo cual atrajo el interés de ciertos grupos religiosos puritanos ingleses. William H. Brock resume muy bien la valía científica del alquimista flamenco en estas palabras: “Pero junto a esta ideología se encontraba la ciencia “positiva” de van Helmont: gases, cuantificaciones y medidas, y la iatroquímica”. Las obras completas del médico y químico de Bruselas, Ortus medicinae (“Orígenes de la medicina”), fueron publicadas en 1648 con este título por su hijo.
Por su parte, Robert Boyle (1627 - 1691), hijo del conde de Cork, es el máximo exponente de la química, como disciplina científica, en el siglo XVII y sus aportaciones experimentales y teóricas (defensor de las interpretaciones mecanicistas y corpusculares de la materia) son de indiscutible valor. En “El químico escéptico” (The Sceptical Chymist; 1661) Boyle exige demostraciones y una rigurosa metodología de trabajo, planteando los experimentos de laboratorio con un meticuloso control de las variables. Es decir, una metodología genuinamente científica. La idea de los cuatro elementos aristotélicos, las explicaciones de los fenómenos físicos mediante “fuerzas ocultas y misteriosas” y los principios de Paracelso (mercurio, azufre y sal “filosóficos”) son atacados por Boyle. Es pues un escepticismo altamente productivo. Se ha dicho que a pesar de la importancia de algunos de los descubrimientos científicos de Boyle (por ejemplo, sus experiencias con los gases) su metodología es de superior relieve.
“El químico escéptico” de Boyle está escrito en forma de diálogo entre un escéptico, un aristotélico, un seguidor de Paracelso y un interlocutor neutral, aunque en su mayor parte es un monólogo del escéptico que expresa las ideas de Boyle. En esta obra fundamental expone Robert Boyle su concepto de elemento. Manifiesta el filósofo de la naturaleza anglo-irlandés: “No veo por qué hemos de creer que existan cuerpos primigenios y simples, a partir de los cuales la naturaleza estuviera obligada a formar todos los demás, como si de elementos preexistentes se tratara”. Para Boyle, los elementos son “ciertos cuerpos primitivos y simples” que “al no estar formados por ningún otro cuerpo, son los ingredientes constitutivos de los que se componen todos aquellos cuerpos denominados perfectamente mixtos, y en los que se descomponen en en última instancia”. En sintonía con la definición de Boyle, hoy se explica a los estudiantes de química que el agua no es un elemento sino un compuesto (una combinación química de elementos) ya que se puede descomponer en sustancias más simples, los elementos que la forman (hidrógeno y oxígeno), mediante electrólisis o descomposición por la corriente eléctrica. Asimismo es destacable la clasificación experimental propuesta por Boyle para distinguir entre soluciones ácidas y alcalinas. Utilizó jarabe de violetas a modo de indicador, ya que observó que viraba hacia el rojo en solución ácida y hacia el verde en medio básico (hoy sabemos que las violetas contienen antocianinas que son pigmentos naturales que cambian su estructura según el pH, provocando cambios de color). A pesar de todo lo anterior, Boyle sigue arrastrando antiguas ideas alquimistas, de hecho siempre estuvo convencido de la posibilidad de transmutación de los metales en oro.
¿Cuál es la aportación española a la nueva química experimental que abandona el hermetismo y que emprende una transición lenta pero progresiva a lo largo del siglo XVII desde los antiguos saberes alquímicos?
A mediados del siglo XVII ve la luz una obra muy importante sobre minería y beneficio de los metales (de tanta importancia práctica). Su autor es Álvaro Alonso Barba (Lepe, Huelva, 1569 - Sucre, 1664), metalúrgico importantísimo en su época. En su célebre Arte de los metales (1640) trata sobre el beneficio del oro y la plata con azogue (mercurio), su fundición, refinado y técnicas de separación. Esta obra es considerada como la más relevante del siglo XVII, a nivel mundial, en minerometalurgia (traducida al inglés, alemán y francés).
Y, ya a comienzos del siglo XVIII, es obligado mencionar a Félix Palacios y Bayá (1677 – 1737), quien introdujo las ideas y conocimientos prácticos de Lemery en España al traducir el importante libro del químico de Rouen (esta primera versión española es de 1703, tan sólo tres años antes de que Palacios publicase su Palestra pharmaceutica, chymico-galenica).
Palacios, como genuino representante del “movimiento novator”, critica la medicina arábigo-galénica imperante y, en la línea de Lemery y los iatroquímicos, propugna la innovación con la aplicación terapéutica de preparados químicos. La Palestra pharmaceutica de Félix Palacios es, sin duda, una obra importante de la literatura científica hispana, la cual sigue un esquema similar al Cours de Chymie de Lemery, de cuyas lecciones aprendió el boticario toledano. El título completo del libro es Palestra pharmaceutica, chymico-galenica. Título significativo, pues de una lucha o discusión se trata: las antiguas concepciones médicas, clásicas, las basadas en las doctrinas de Galeno, frente a las modernas o iatroquímicas. Se públicó por primera vez la Palestra pharmaceutica en 1706 y tuvo varias ediciones a lo largo de todo el siglo XVIII. El imprescindible libro de Palacios, en la edición de 1737, lleva el siguiente subtítulo, casi un prólogo: “ En la cual se trata de la elección de los simples, sus preparaciones químicas, y galénicas, y de las más selectas composiciones antiguas, y modernas, usuales, tanto en Madrid, como en toda Europa, descritas por los antiguos, y modernos, con las anotaciones necesarias, y más nuevas, que hasta lo presente se han escrito, tocantes a su perfecta elaboración, virtudes, y mejor aplicación en los enfermos. Obra muy útil, y necesaria para todos los profesores de la Medicina, médicos, cirujanos, y en particular boticarios: muy añadida en esta tercera impresión”. También pues, en nuestro país, no sin la oposición de los núcleos académicos más reticentes a la modernización, comenzaba a surgir una química más racional y experimental que pretendía dejar atrás los saberes clásicos.
BIBLIOGRAFÍA:
- ASIMOV, Isaac; Enciclopedia biográfica de Ciencia y Tecnología; Alianza Editorial, Madrid, 1987.
- BLAS, L. Biografías y descubrimientos químicos; Aguilar Ed. Madrid, 1947.
- BROCK, William H. Historia de la química; Alianza Editorial, Madrid, 1998.
- REICHEN, Charles Albert; Historia de la química (Historia ilustrada de las ciencias y de las invenciones); Editorial Continente, Madrid, 1965.
En Internet:
- RIVERO, Bernardo; La Química a la palestra. Una aproximación a los orígenes de la ciencia química en España; El rincón de la ciencia:
http://centros5.pntic.mec.es/ies.victoria.kent/Rincon-C/Curiosid2/rc-101/rc-101a.htm






.jpg/1920px-Mar%C3%ADa_Cegarra_(20211220_100524).jpg?20211227232911)







